Như các em đã biết, nguyên tử có khả năng liên kết với nhau và hóa trị là con số thể hiện khả năng đó, khi biết hóa trị của một nguyên tố ta sẽ lập được công thức hóa học của hợp chất.
Vậy hóa trị là gì? Quy tắc, cách tính hóa trị của nguyên tố hay nhóm nguyên tử được vận dụng như thế nào? Hóa trị của Cu, Ag,… cùng một số kim loại, phi kim phổ biến là bao nhiêu trong bảng hóa trị nguyên tố hóa học? chúng ta cùng tìm hiểu qua bài viết này.
I. Hóa trị của một nguyên tố được xác định bằng cách nào?
1. Cách xác định hóa trị của một nguyên tố
– Quy ước: Gán cho H hóa trị I, chọn làm đơn vị.
– Một nguyên tử nguyên tố khác liên kết được với bao nhiêu nguyên tử hidro thì nói nguyên tố đó có hóa trị bằng bấy nhiêu.
* Ví dụ: HCl: Clo hóa trị I;
H2O: Oxi hóa trị II
NH3: Nitơ hóa trị III
CH4: Cacbon hóa trị IV
– Dựa vào khả năng liên kết của các nguyên tố khác với O (Hóa trị của oxi bằng 2 đơn vị, Oxi có hóa trị II).
* Ví dụ: K2O: K có hóa trị I
CaO: Ca có hóa trị II
SO2: S có hóa trị IV
CuO thì Cu có hóa trị II
Ag2O thì Ag có hóa trị I
* Hóa trị của nhóm nguyên tử
* Ví dụ: H2SO4 thì nhóm SO4 có hóa trị II
HNO3 thì nhóm NO3 có hóa trị I
H3PO4 thì nhóm PO4 có hóa trị III
HOH thì nhóm OH có hóa trị I
2. Kết luận
– Hóa trị là con số biểu thị khả năng liên kết của nguyên tử nguyên tố này với nguyên tử nguyên tố khác.
– Hóa trị của một nguyên tố được xác định theo hóa trị của H chọn làm đơn vị (H hóa trị I) và hóa trị của O là hai đơn vị (O hóa trị II).
– Hóa trị của một nhóm nguyên tố cũng tương tự như trên (nhóm nguyên tử được coi như một nguyên tố bất kỳ).
* Lưu ý: Có những nguyên tố chỉ thể hiện một hóa trị nhưng cũng có những nguyên tố có một vài hóa trị khác nhau.
II. Quy tắc, cách tính hóa trị của nguyên tố hóa học
1. Quy tắc hóa trị
– Công thức hóa học của hợp chất 2 nguyên tố bất kỳ: 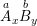
Trong đó: (x, y) là chỉ số; (a,b) là hóa trị của các nguyên tố
• Trong công thức hóa học, tích của chỉ số và hóa trị của nguyên tố này bằng tích của chỉ số và hóa trị của nguyên tố kia.
– Công thức tổng quát: 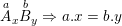
• Như vậy, theo quy tắc hóa trị thì: a.x = b.y
– Nếu biết x, y và a thì ta tính được 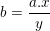
– Nếu biết x, y và b thì ta tính được 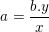
– Nếu biết a, b thì ta tính được x, y để lập công thức hóa học bằng cách lập tỉ lệ:
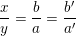 (b’/a’ là rút gọn của b/a nếu có).
(b’/a’ là rút gọn của b/a nếu có).
– Lấy x = b (hay b’) và y = a (hay a’);
2. Vận dụng quy tắc tính hóa trị để tính hóa trị của một nguyên tố và lập công thức hóa học của hợp chất theo hóa trị.
a) Tính hóa trị của một nguyên tố
* Ví dụ: Tính hóa trị của Fe trong hợp chất FeCl3, cho biết clo hóa trị I
– Gọi hóa trị của Fe là a, ta có: 1.a = 3.I ⇒ a = III.
– Tương tự, ta có:
AgCl: 1.a = 1.I ⇒ a= I; vậy Ag có hóa trị I
CuCl2: 1.a = 2.I ⇒ a = II; Vậy Cu có hóa trị II
AlCl3: 1.a = 3.I ⇒ a = III; Vậy Al có hóa trị III
b) Lập công thức hóa học của hợp chất theo hóa trị
* Ví dụ 1: Lập công thức hóa học của hợp chất tạo bởi lưu huỳnh VI và Oxi
– Công thức tổng quát dạng: SxOy
– Theo quy tắc hóa trị: x.VI = y.II
– Ta lập tỉ lệ: 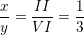
– Thường thì tỉ lệ số nguyên tử trong phân tử là những số nguyên đơn giản nhất, vì vậy lấy: x = 1 và y = 3.
⇒ Công thức hóa học của hợp chất: SO3
* Ví dụ 2: Lập công thức hóa học của hợp chất tạo bởi Kali hóa trị I và nhóm SO4 hóa trị II
– Viết công thức chung: Kx(SO4)y
– Theo quy tắc hóa trị: x.I = y.II
– Lập tỉ lệ: 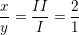
⇒ Công thức hóa học của hợp chất: K2SO4

• Bảng hóa trị của một số nguyên tố hóa học phổ biến
|
Tên Nguyên tố |
Ký hiệu hoá học |
Hoá trị |
Nguyên tử khối |
Số proton |
|
Hiđro |
H |
I |
1 |
1 |
|
Heli |
He |
|
4 |
2 |
|
Liti |
Li |
I |
7 |
3 |
|
Beri |
Be |
II |
9 |
4 |
|
Bo |
B |
III |
11 |
5 |
|
Cacbon |
C |
IV, II |
12 |
6 |
|
Nitơ |
N |
II, III, IV,… |
14 |
7 |
|
Oxi |
O |
II |
16 |
8 |
|
Flo |
F |
I |
19 |
9 |
|
Neon |
Ne |
|
20 |
10 |
|
Natri |
Na |
I |
23 |
11 |
|
Magie |
Mg |
II |
24 |
12 |
|
Nhôm |
Al |
III |
27 |
13 |
|
Silic |
Si |
IV |
28 |
14 |
|
Photpho |
P |
III, V |
31 |
15 |
|
Lưu huỳnh |
S |
II, IV, VI |
32 |
16 |
|
Clo |
Cl |
I,… |
35,5 |
17 |
|
Argon |
Ar |
|
39,9 |
18 |
|
Kali |
K |
I |
39 |
19 |
|
Canxi |
Ca |
II |
40 |
20 |
|
Crom |
Cr |
II, III |
52 |
24 |
|
Mangan |
Mn |
II, IV, VII,… |
55 |
25 |
|
Sắt |
Fe |
II, III |
56 |
26 |
|
Đồng |
Cu |
I, II |
64 |
29 |
|
Kẽm |
Zn |
II |
65 |
30 |
|
Brom |
Br |
I,… |
80 |
35 |
|
Bạc |
Ag |
I |
108 |
47 |
|
Bari |
Ba |
II |
137 |
56 |
|
Thuỷ ngân |
Hg |
I, II |
201 |
80 |
|
Chì |
Pb |
II, IV |
207 |
82 |
• Hóa trị của một số nhóm nguyên tử hóa học
– Nhóm Hóa trị I: Hiđroxit (dùng trong hợp chất với kim loại) (OH); Nitrat (NO3); Clorua (Cl);
* Ví dụ: NaOH (bazơ mạnh) ; HNO3 (axit mạnh); HCl (axit mạnh)
– Nhóm Hóa trị II: Sunfat (SO4); Cacbonat (CO3);
* Ví dụ: H2SO4 (axit mạnh); H2CO3 (axit yếu, dễ bị phân ly)
– Nhóm hóa trị III: Photphat (PO4);
* Ví dụ: H3PO4 (axit trung bình)
III. Bài tập về hóa trị của nguyên tố hóa học
* Bài 1 trang 37 SGK Hóa 8: a) Hóa trị của một nguyên tố (hay nhóm nguyên tử) là gì?
b) Khi xác định hóa trị, lấy hóa trị của nguyên tố nào làm đơn vị, nguyên tố nào là hai đơn vị?
° Lời giải bài 1 trang 37 SGK Hóa 8:
a) Hóa trị của nguyên tố (hay nhóm nguyên tử) là con số biểu thị khả năng liên kết của nguyên tử (hay nhóm nguyên tử).
b) Khi xác định hóa trị lấy hóa trị của H làm đơn vị và hóa trị của O là hai đơn vị.
* Bài 2 trang 37 SGK Hóa 8: Hãy xác định hóa trị của mỗi nguyên tố trong các hợp chất sau đây:
a) KH, H2S, CH4.
b) FeO, Ag2O, SiO2.
° Lời giải bài 2 trang 37 SGK Hóa 8:
a) KH, H2S, CH4.
◊ 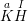 : với a là hóa trị của K
: với a là hóa trị của K
– Theo quy tắc hóa trị, ta có: 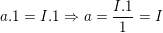
⇒ Vậy hóa trị của K là I
◊ 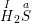 : với a là hóa trị của S
: với a là hóa trị của S
– Theo quy tắc hóa trị, ta có: 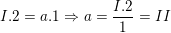
⇒ Vậy hóa trị của S là II
◊ 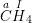 : với a là hóa trị của C
: với a là hóa trị của C
– Theo quy tắc hóa trị, ta có: 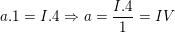
⇒ Vậy hóa trị của C là IV
b) FeO, Ag2O, SiO2.
◊ 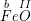 : gọi b là hóa trị của Fe
: gọi b là hóa trị của Fe
– Theo quy tắc hóa trị, ta có: 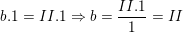
⇒ Vậy hóa trị của Fe là II
◊ 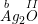 : với b là hóa trị của Ag
: với b là hóa trị của Ag
– Theo quy tắc hóa trị, ta có: 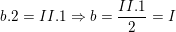
⇒ Vậy hóa trị của Ag là I
◊ 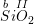 : với b là hóa trị của Si
: với b là hóa trị của Si
– Theo quy tắc hóa trị, ta có: 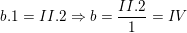
⇒ Vậy hóa trị của Si là IV
* Bài 3 trang 37 SGK Hóa 8: a) Nêu quy tắc hóa trị với hợp chất hai nguyên tố. Lấy công thức hóa học của hai hợp chất trong câu 2 làm thí dụ.
b) Biết công thức hóa học K2SO4 trong đó có K hóa trị I, nhóm (SO4) hóa trị II. Hãy chỉ ra là công thức hóa học trên phù hợp đúng theo quy tắc hóa trị.
° Lời giải bài 3 trang 37 SGK Hóa 8:
a) Quy tắc hóa trị với hợp chất hai nguyên tố: Trong công thức hóa học, tích của chỉ số và hóa trị của nguyên tố này bằng tích của chỉ số và hóa trị của nguyên tố kia.
* Lấy ví dụ theo bài 2 ta có:
– FeO: Fe hóa trị II, oxi cũng hóa trị II ⇒ II.1 = 1.II
– SiO2: Si hóa trị IV, oxi hóa trị II ⇒ IV.1 = II.2
b) Vì K hóa trị I, nhóm SO4 hóa trị II
– Theo quy tắc hóa trị: 2.I = 1.II.
⇒ Công thức K2SO4 là công thức phù hợp với quy tắc hóa trị.
* Bài 8 trang 38 SGK Hóa 8: a) Tìm hóa trị của Ba và nhóm (PO4) trong bảng 1 và bảng 2 (trang 42, 43)
b) Hãy chọn công thức hóa học đúng trong các công thức sau đây:
A. BaPO4 B.Ba2PO4. C.Ba3PO4. D.Ba3(PO4)2.
° Lời giải bài 8 trang 38 SGK Hóa 8:
a) Hóa trị của Ba là II và nhóm (PO4) bằng III
b) Chọn đáp án: D. Ba3(PO4)2.
– Gọi công thức dạng chung của Ba(II) và nhóm PO4 (III) là 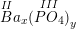
– Theo quy tắc hóa trị ta có:
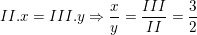
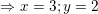
⇒ Công thức hóa học là Ba3(PO4)2.
Hy vọng bài viết đã giúp các em hiểu Hóa trị là gì? và biết Quy tắc, cách tính hóa trị của nguyên tố, nhóm nguyên tử hóa học và Bảng hóa trị. Trường TCSP Mẫu giáo – Nhà trẻ Hà Nội chúc các em học tốt và đừng quên để lại góp ý hay thắc mắc dưới phần nhận xét nhé.
|
¤ Các bài viết cùng Chương 1: ¤ Có thể bạn muốn xem: |